【互联网 www.tofms.org】 【My Blog】
如需转载本站内容,请注明资料来源于: www.tofms.org
|
| 【技术】【旧文】蛋白质药物降解比你想象的复杂多了 |
从本人曾经的微信公众号文章找回。
是目标蛋白的降解?还是宿主细胞蛋白残余?
每个条带是不是唯一降解?
降解位点在哪里?
降解机制可能是哪种?
我们曾经开发了一套完整的降解物解析方案,包括多种样本前处理,多层次、多水平、多种检测方式相结合,获得了大量十分有参考价值的数据和结果。 大量降解研究结果显示,单一降解位点的情况较少,一个条带一般含有3~5种以上不同降解的情况,甚至没有主要位点。图1是某重组药物的结果,串联质谱鉴定其降解较单纯:双链中的某一条链发生特异性酶解(来自表达体系),且与空间构象密切相关。 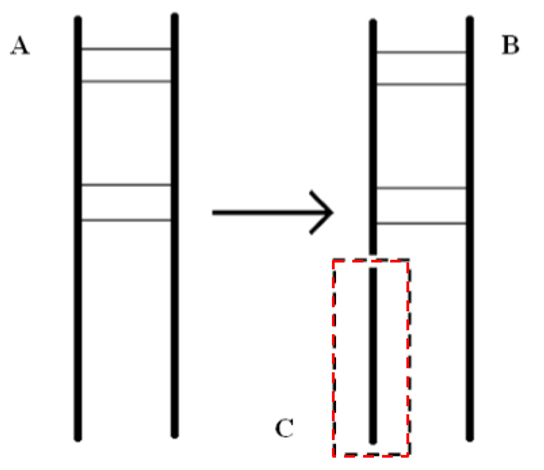 图1 某蛋白药物简单降解例子 在我们的实践中,疫苗的降解非常普遍,有些疫苗降解产物较单纯,有些疫苗降解产物非常复杂(如乙肝疫苗)。HPV疫苗18L1的降解有一定特点(图2)。不同条带均有主要降解位点,如D432、K360、K278、D240,但每个条带都不是单一的剪切蛋白,它主要包含C-端剪切形式,还包含其他剪切方式:N端剪切和中间剪切。 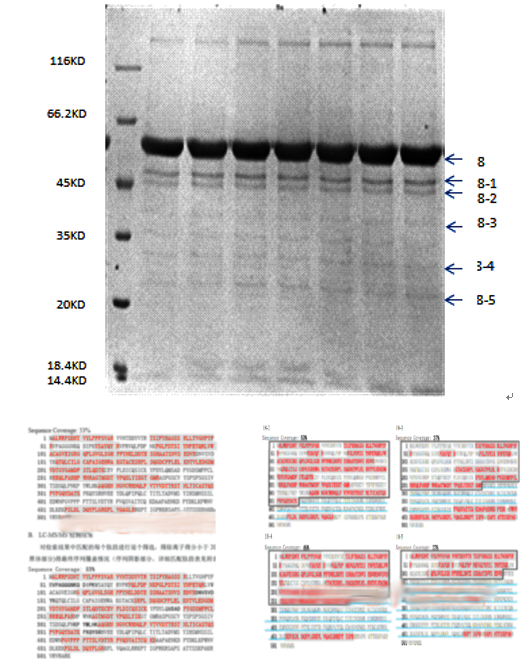 图2 某HPV18L1降解例子 如今质谱技术越来越先进,分子量测定也越来越精确,但对于想快速判断降解位点的企图来说,精确度远远不够。图3是最近我们解析的某药物23kDa条带的情况。质谱获得了该条带内3个组分的分子量,通过分析发现有50个候选序列的偏差小于20ppm,小于10ppm者也有32个。对于1个23kDa的蛋白,即使FT-ICR-MS,要达到10ppm的准确度,并不是件容易的事。你只要看看校正仪器时的准确度就可以知道(不是标准肽校正哦)。质谱仪器验收指标里的内标0.5ppm和外标1ppm,那是小分子或小肽,不是蛋白。在降解分析时,质谱分子量是非常重要的,它能可靠的测出组分数量和分子量范围,是解析C-末端最核心数据之一,但质谱分子量解析降解产物又是十分有限的。 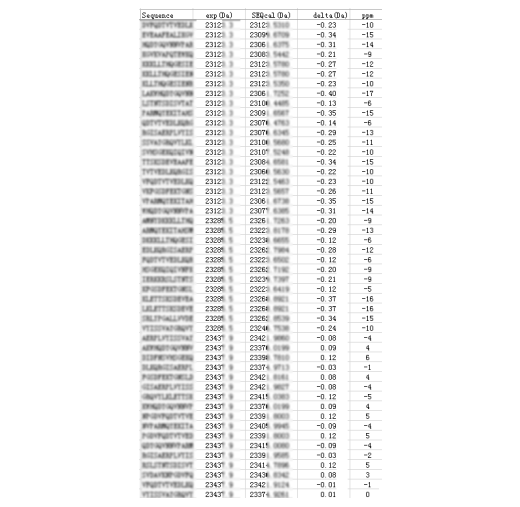 图3 某药物23kDa条带解析例子 我们在有限的研究中发现,有少数特异性酶切位点,这类降解发生在发酵过程中,与发酵体系密切相关,蛋白降解酶一般是宿主细胞分泌的,基本上难以避免,除非添加相关蛋白酶抑制剂。更多的情况是,胞内酶解和水解共存。水解是随机的,与发酵体系的温度、pH、时间、Buffer类型有关,跟细胞似乎关系不大。通过跟踪纯化过程的产物,我们也很惊喜的发现,纯化工艺很少发生再次降解,应该是与大家良好的纯化理念有关。 总之,降解是重组药物司空见惯的事情,大家首先一定要去研究它,最后能较深入研究,要合理控制比例且保持批间一致性。万一宿主细胞蛋白与降解产物混在一起,那得十分严肃认真对待了,具体怎么办,我们可以好好讨论讨论。 更多精彩文章,请关注公众号 【药网堂】 All rights reserved , visit the micromessage 药网堂 for more @ tofms_org@126.com  【wkh, 2024-05-28 14:19:33】 【责任人 wkh】 [已阅读 368 次] |
Email:tofms_org@126.com 【有疑问,发邮件】 © 2008- All Rights Reserved, Powered by WKH© 2008 |